| Trial Protocole | Back |
Conception de l'étude.
| Résumé |
|
CRASH est une expérience
simple et à grande échelle, avec un contrôle placebo,
portant sur les effets d'une perfusion de corticostéroïdes
pendant 48 heures sur la mortalité et sur les incapacités
neurologiques, parmi les adultes et une certaine perte de connaissance.
Les procédures sont décrites à la Figure 2, et
au dos du protocole. Les patients souffrant de blessures à la
tête et ayant perdu connaissance, âgés de 16 ans
ou plus, sont éligibles si le médecin traitant est, pour
une raison quelconque, plus qu'hésitant sur l'utilisation ou
non de corticostéroïdes. Des packs numérotés
de médicaments ou de placebo seront disponibles dans chaque Service
d'urgence participant. La randomisation englobe le fait d'appeler un
service téléphone gratuit ouvert 24 heures sur 24. L'appel
ne devrait pas dépasser une ou deux minutes et à la fin
de la communication, le service indiquera à la personne appelant
le numéro du pack de traitement à utiliser. Le médicament
ou le placebo dans le pack conditionné dans une solution saline
et, avec une dose de base d'une heure, doit être administré
par perfusion pendant 48 heures (ou une durée s'en rapprochant
autant que possible). Aucun autre essai n'est requis, mais il faut remplir
un bref formulaire 2 semaines plus tard (ou bien après un décès
ou la sortie du malade de l'hôpital). |
| Nombre de patients nécessaires |
|
Deux principaux facteurs déterminent le nombre de patients nécessaires dans une expérience. Il s'agit de l'estimation de la fréquence des événements et du niveau d'efficacité du traitement... |
|
Estimation
de la fréquence des événements: Dans
une récente expérience randomisée englobant plusieurs
centres et portant sur les blessures à la tête avec des
critères d'inclusion similaires à ceux de l'expérience
CRASH, le risque global de mortalité parmi les patients de référence
était de 15%, avec le risque de résultat défavorable
(décès, incapacité de travail ou besoin de rééducation)
égal à 43%.[Ref
12] Cette expérience est l'une des expériences
randomisées les plus récentes de corticostéroïdes
dans les blessures à la tête et il serait raisonnable de
compter sur un risque similaire de résultat défavorable
dans l'expérience CRASH... |
|
Niveau
d'efficacité de traitement devant être détectable:
Parce que même un taux de survie
de 2% pour une intervention aussi simple et largement utilisable que
les corticostéroïdes représenterait un avantage valable,
l'expérience actuelle a été planifiée pour
détecter un avantage de cette ampleur. |
|
Nombres
nécessaires: Si la différence
de mortalité réelle est 15% par rapport à 13% il
y aurait alors 65% de chances qu'une expérience impliquant 10.000
patients atteindrait 2P<0.01, et 95% de chances qu'une expérience
impliquant 20.000 patients en fasse autant. Ces calculs évaluent
la vulnérabilité de l'expérience aux aléas.
Si malgré tout, comme cela pourrait être le cas, les résultats
proprement dits ne sont pas beaucoup faussés par les aléas
et impliquant un taux de mortalité de 15% par rapport à
13%, alors une expérience de 10.000 donnerait 2P=0,004, et une
expérience de 20.000 donnerait 2P=0.00004 (résultat suffisamment
extrême pour permettre des analyses annexes exploratrices dont
les types de patients ont le plus de chances de bénéficier. |
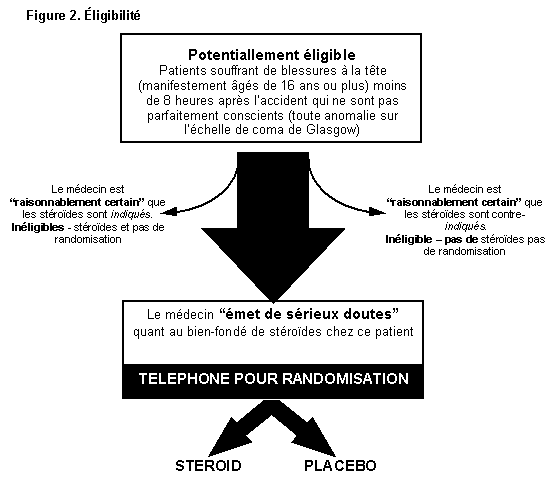
| Eligibilité |
Les
patients souffrant de blessures à la tête (âgés
de 16 ans ou plus) dans les 8 heures suivant les blessures qui ne sont
pas parfaitement conscients (toute anomalie sur l'échelle de
coma de Glasgow), à l'exception de ceux pour lesquels les corticostéroïdes
sont censés être clairement indiqués ou contre-indiqués
|
|
Tous
les patients blessés à la tête qui, en l'absence
de sédation, présentent à l'hôpital un GCS
inférieur ou égal à 14, moins de 8 heures après
l'accident, sont éligibles pour participer à l'expérience
s'ils paraissent âgés de 16 ans au moins. Même si
la participation admet des patients blessés à la tête
plus de 8 heures plus tôt, plus le traitement intervient à
un stade précoce, plus l'efficacité sera importante... |
|
Il
n'y a pas d'autre critère d'exclusion prédéterminé
dans la mesure où le critère d'éligibilité
fondamental est l'incertitude' du médecin traitant quant à
l'utilisation de corticostéroïdes chez un adulte particulier
souffrant de blessures à la tête.[Ref
13] Les patients que le médecin traitant considère
comme indiqués pour les corticostéroïdes (comme par
exemple les patients souffrant de graves blessures de la moelle épinière)
ne doivent pas être randomisés. De même, les patients
que le médecin traitant considère comme contre-indiqués
pour les corticostéroïdes ne doivent pas être randomisés.
Mais tous les patients pour lesquels le médecin traitant ne sait
pas s'il convient de donner des corticostéroïdes sont éligibles
pour la randomisation, et il convient de considérer le plus grand
nombre de patients pour l'expérience. |
|
L'hétérogénéité des types de patients participant à l'expérience est une force scientifique, et non une faiblesse. Si une vaste gamme de patients est randomisée, une expérience réelle d'une telle échelle devrait contribuer à déterminer les types particuliers (le cas échéant) devant le mieux bénéficier du traitement... |
 |
|
Considérations
spéciales d'éligibilité: Aucune. L'exclusion
de routine de patients souffrant de problèmes gastro-intestinaux
ou les femmes enceintes n'est pas nécessaire, sauf si le médecin
traitant considère qu'il s'agit sans conteste d'une contre-indication. |
|
Notes: |
| Consentement |
|
Les
patients souffrant de blessures à la tête et ayant perdu
connaissance ne seront pas toujours en mesure de formuler leur consentement,
et dans cette situation d'urgence, il ne sera pas forcément indiqué,
du point de vue médical, de différer le début du
traitement jusqu'à l'obtention du consentement par une personne
habilitée en ce sens. C'est la raison pour laquelle le médecin
chargé du malade devrait prendre la responsabilité de
l'admission desdits patients, comme il le ferait pour choisir d'autres
thérapies. Toutefois, les exigences du comité d'éthique
compétent devraient être respectées en permanence.
Une brochure d'information sur l'étude pour les patients et leurs
amis et les membres de leur famille sera disponible dans tous les packs
de médicaments [Annexe
1]. |
|
Les
patients éligibles pour inclusion devraient être randomisé,
et le traitement de l'étude commencé dans les meilleurs
délais,. La randomisation s'effectue par téléphone,
avec un service gratuit ouvert 24 heures sur 24, et ne prend que deux
minutes environ. Le formulaire d'inscription des patients [Annexe
2] montre les questions qui seront posées par l'opérateur
téléphonique avant d'allouer les packs de traitement.
L'ordinateur de l'étude va ensuite assigner de façon aléatoire
un numéro de pack de traitement identifiant un pack de traitement
CRASH stocké dans le service d'urgence. Une fois qu'un patient
a été randomisé, nous espérons vivement
suivre son évolution à l'hôpital, même si
le traitement de l'expérience est interrompu, voire même
n'est pas administré. |
| Traitement de l'étude |
| Chaque pack de traitement CRASH contient: |
|
| Traitement |
|
Dose (MP ou placebo) |
| Base |
|
2g pendant 1 heure |
| Jour 1 |
|
0,4 g/heure pendant ~24 heures |
| Jour 2 |
|
0,4 g/heure pendant ~24 heures |
Base |
|
2g MP (ou placebo équivalent) pendant 1 heure dans une de perfusion de 100 mL: |
|
1.
Ajouter 20 mL d'eau pour injection dans un flacon de 2g et bien mélanger |
Maintenance quotidienne |
| 0,4g/heure pendant environ 24 heures dans une perfusion de 20 mL/heure (MP ou placebo équivalent): |
|
1.
Retirer 100mL d'un sachet de 500 mL de 0,9% de NaCl (pour faire de la
place pour le stéroïde) |
|
Nota.
Comme les enfants âgés de moins de 16 ans sont exclus de
l'expérience, on peut utiliser un simple traitement à
dose fixe. La posologie est celle des expériences NASCIS-2 et
NASCIS-3 de MP dans les graves blessures de la moelle épinière. |
| Evénements adverses inattendus |
|
Les
réactions anaphylactiques aux corticostéroïdes intraveineux
sont extrêmement rares, mais devraient être traités
de la façon préconise par le médecin responsable
(une possibilité étant l'adrénaline intramusculaire
de 0,5mg, c'est-à-dire 0,5 mL de 1 dans une solution de 1.000
(1mg/mL) ).[Ref 14]
On pense qu'une couverture anesthésique de 24 heures serait disponible
dans tous les hôpitaux participant à l'expérience
CRASH.
|
|
En
règle générale, il n'est pas nécessaire
de signaler de cette façon les infections et les saignements
gastro-intestinaux parce que l'on pourrait s'attendre à une incidence
croissante pour les stéroïdes. De même, les divers
événements médicaux auxquels on pourrait s'attendre
chez les patients blessés à la tête n'ont pas besoin
d'être signalés par téléphone. Tous les événements
de cette nature sont surveillés de façon systématique
pour tous les patients sur le formulaire des résultats. |
| 'Interruption' en urgence du traitement prévu |
|
En règle
générale, il ne devrait y avoir aucune raison d'interrompre
le traitement prévu. Si une certaine contre-indication pour les
corticostéroïdes apparaît après la randomisation
(par exemple un saignement gastro-intestinal important), il convient
tout simplement d'arrêter le traitement de l'expérience.
L'interruption n'est jamais apparue nécessaire dans l'expérience
NASCIS de MP pour les blessures de la moelle épinière,4
et ne devrait se produire que dans les rares cas dans lesquels le médecin
pense que la gestion clinique dépend dans une grande mesure du
fait que l'on sait si le patient à reçu un corticostéroïde
ou un placebo (par exemple si l'on redoute une anaphylaxis). Dans les
très rares cas dans lesquels on considère une interruption
urgente comme nécessaire, il convient de téléphoner
au service de randomisation , en indiquant le nom du médecin
autorisant l'interruption et le numéro de pack de traitement
CRASH (s'il est connu), et la personne appelant saura si le patient
a reçu un corticostéroïde ou un placebo. |
| Les
résultats de mesure initiaux sont: .. |
|
| Les
mortalités à l'hôpital, les complications et le rétablissement
à court terme doivent être consignés sur le formulaire
de résultat initial qui peut être rempli entièrement
à partir des notes prises à l'hôpital, sans examens
supplémentaires. .. |
| Le
rétablissement à long terme sera évalué au
bout de six mois soit sous forme d'un simple questionnaire adressé
par la poste, envoyé directement à chaque participant à
l'expérience depuis le Centre de coordination CRASH, soit sous
forme d'entretien téléphonique. Ceci n'implique pas de travail
supplémentaire pour les hôpitaux participant à l'expérience. |
| Analyse |
|
Des comparaisons seront faites à partir des premières mesures de résultats, entre les patients traités à la méthylprednisolone et les patients ayant reçu un placebo, sur une base dite de 'volonté de traitement'. Les analyses seront échelonnées dans le temps entre le moment de la blessure et le début du traitement, et également en fonction de la gravité de la blessure à la tête évaluée par l'Echelle de coma de Glasgow. Des comparaisons seront également réalisées quant aux risques d'infection et de saignement gastro-intestinal. |