| Trial ProtoKoll | Back |
Studienaufbau.
| Überblick |
|
CRASH
ist ein großer, einfacher Versuch mit Placebokontrolle über
die Auswirkungen einer 48-stündigen Infusion von Corticosteroiden
auf die Zahl der Todesfälle und neurologische Leiden bei Erwachsenen
mit Kopfverletzung und in gewissem Maße beeinträchtigtem
Bewusstseinszustand. Die Verfahren sind in Abbildung 2 und auf der Rückseite
des Protokolls beschrieben. Patienten mit Kopfverletzungen mit beeinträchtigtem
Bewusstseinszustand, deren Alter auf 16 Jahre oder älter geschätzt
wird, sind für die Teilnahme geeignet, wenn der verantwortliche
Arzt sich, egal aus welchem Grund, in hohem Maße unsicher ist,
ob er Corticosteroide verwenden soll oder nicht. Nummerierte Arzneimittel-
oder Placebopackungen werden in jeder teilnehmenden Notaufnahme-Abteilung
bereitstehen. Die Randomisierung erfolgt über den Anruf bei einer
gebührenfreien, rund um die Uhr erreichbaren Telefonnummer. Der
Anruf sollte nur ein oder zwei Minuten dauern, und am Ende des Anrufs
gibt der Telefondienst dem Anrufer an, welche der nummerierten Behandlungspackungen
zu verwenden ist. Das Arzneimittel oder Placebo in der Packung befindet
sich in Salzlösung und wird nach einer einstündigen Initialdosis
über 48 Stunden (oder über einen Zeitraum, der so nahe an
48 Stunden liegt wie möglich) als Infusion verabreicht. Es sind
keine zusätzlichen Untersuchungen erforderlich, aber 2 Wochen später
(oder nach vorherigem Tod oder vorheriger Entlassung) muss ein kurzes
Formular ausgefüllt werden. |
| Anzahl benötigter Patienten |
|
Zwei Hauptfaktoren bestimmen die Anzahl benötigter Patienten in einem Versuch: die geschätzte Vorkommnisrate und die Größe des Behandlungseffekts. |
|
Größe des Behandlungseffekts, der erkennbar sein sollte: Weil selbst eine nur um 2% erhöhte Überlebenschance durch eine so einfache breit anwendbare Maßnahme wie Corticosteroide einen lohnenden Vorteil darstellen würde, wurde der aktuelle Versuch so geplant, dass ein Vorteil dieser Größe feststellbar ist. Benötigte
Patientenzahlen: Wenn die tatsächliche Differenz der Sterblichkeitsrate
15% zu 13% ist, sollte es eine 65%ige Chance geben, dass ein Versuch
mit 10 000 Patienten 2P<0,01 erreicht, und eine 95%ige Chance, dass
ein Versuch mit 20 000 Patienten dies erreicht. Mit diesen Berechnungen
wird abgeschätzt, wie gut der Versuch gegen widrige Zufälle
geschützt ist. Wenn jedoch, was sehr wohl der Fall sein kann, die
tatsächlichen Ergebnisse vom Zufall nicht sehr verzerrt werden
und eine Sterblichkeitsrate von 15% versus 13% beinhalten, würde
ein Versuch mit 10 000 Patienten 2P=0,004 ergeben, und ein Versuch mit
20 000 Patienten würde 2P=0,00004 ergeben (was extrem genug ist,
um einige explorative Subanalysen darüber zu erstellen, für
welche Patiententypen ein Vorteil am wahrscheinlichsten ist). |
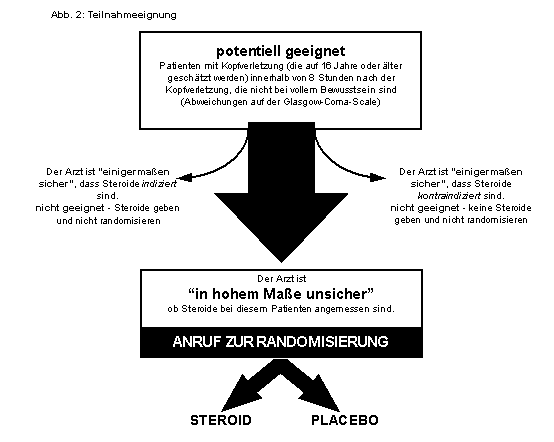
| Teilnahmeeignung |
Patienten mit Kopfverletzungen (die auf 16 Jahre oder älter geschätzt werden) innerhalb von 8 Stunden nach der Verletzung, die nicht bei vollem Bewusstsein sind (jede Abweichung auf der Glasgow-Coma-Scale), mit Ausnahme derjenigen, bei denen Corticosteroide für klar indiziert oder kontraindiziert gehalten werden. |
|
Alle
Patienten mit Kopfverletzungen, bei denen ¾ ohne Sedierung ¾
im Krankenhaus eine GCS (Glasgow-Coma-Scale) von 14 oder weniger beobachtet
wird, und bei denen nicht mehr als 8 Stunden seit der Verletzung vergangen
sind, eignen sich für die Teilnahme am Versuch, wenn sie mindestens
16 Jahre alt zu sein scheinen. Wenngleich eine Teilnahme an der Studie
bis zu 8 Stunden nach der Verletzung erlaubt ist, ist es besser, wenn
die Patienten so früh wie möglich behandelt werden können. Die Heterogenität
der Patiententypen, die an so einem Versuch teilnehmen, ist wissenschaftlich
gesehen eine Stärke, keine Schwäche. Wenn eine große
Bandbreite von Patienten randomisiert wird, kann ein wirklich großer
Versuch wie dieser eventuell mit dazu dienen, zu bestimmen, welche spezifischen
Patiententypen (wenn überhaupt welche) am wahrscheinlichsten von
der Behandlung profitieren.
|
 |
|
Besondere
Eignungskriterien: Keine. Eine routinemäßiger Ausschluss
von Patienten mit Magen-Darm-Beschwerden oder Schwangerschaft ist nicht
erforderlich, da der verantwortliche Arzt dies als eindeutige Kontraindikation
bewertet. |
|
Hinweise: |
| Einverständnis |
|
Patienten
mit Kopfverletzung und beeinträchtigtem Bewusstseinszustand können
nicht in der Lage sein, ihre ordnungsgemäße informierte Einwilligung
zu geben, und in dieser Notsituation kann es medizinisch nicht angebracht
sein, mit dem Beginn der Behandlung zu warten, bis die Einwilligung
einer bevollmächtigten Person eingeholt werden kann. Daher muss
der verantwortliche Arzt die Verantwortung übernehmen, solche Patienten
in die Studie einzuschließen, wie er auch für die Wahl anderer
Behandlungen die Verantwortung übernimmt. Die Anforderungen der
zuständigen Ethik-Kommission sind allerdings stets einzuhalten.
Ein Informationsblatt über die Studie für Patienten und ihre
Freunde und Verwandten wird allen Arzneimittelpackungen beiliegen [Anhang
1]. |
|
Patienten,
die sich für die Teilnahme an der Studie eignen, sind zu randomisieren,
und mit der Versuchsbehandlung ist so bald wie möglich zu beginnen.
Die Randomisierung erfolgt über einen Anruf bei einer rund um die
Uhr erreichbaren gebührenfreien Telefonnummer und dauert nur etwa
2 Minuten. Im Patienten-Aufnahmeformular [Anhang
2] stehen die Fragen, die vom Telefondienst vor der Zuweisung
der Behandlungspackungen gestellt werden. Der Computer für die
Studie weist dann nach dem Zufallsprinzip eine Behandlungspackungsnummer
zu, die eine der CRASH-Behandlungspackungen bezeichnet, die in der Notaufnahme-Abteilung
gelagert sind. Wenn ein Patient randomisiert wurde, möchten wir
auf jeden Fall über das Behandlungsergebnis im Krankenhaus informiert
werden, selbst wenn die Behandlung unterbrochen wird oder doch nicht
durchgeführt wird. |
| Studien-Behandlung |
| Jede CRASH-Behandlungspackung enthält: |
|
| Behandlung |
|
Dosis (MP oder Placebo) |
| Initialdosis |
|
2g über 1 Stunde |
| 1. Tag |
|
0,4 g/Stunde, ~24 Stunden lang |
| 2. Tag |
|
0,4 g/Stunde, ~24 Stunden lang |
Initialdosis |
|
2g MP (oder die entsprechende Placebomenge) über 1 Stunde verteilt in 100ml Infusion: |
|
|
Tägliche Erhaltungsdosis |
| 0,4g/Stunde über etwa 24 Stunden verteilt in einer Infusion von 20 ml/Stunde (MP oder die entsprechende Placebomenge): |
|
|
| Unerwartete Nebenwirkungen |
|
Anaphylaktische Reaktionen auf intravenöse Corticosteroide sind extrem selten, aber sind in der vom verantwortlichen Arzt vorgezogenen Weise zu behandeln (eine Möglichkeit ist die intramuskuläre Gabe von Adrenalin 0,5mg, d.h. 0,5ml einer 1:1000 verdünnten Lösung (1mg/ml)).[Ref 14] Es wird vorausgesetzt, dass Anästhetikum für 24 Stunden in allen Krankenhäusern verfügbar ist, die an CRASH teilnehmen. Wenn schwere und unerwartete Arzneimittelnebenwirkungen auftreten und der Verdacht besteht, dass sie mit dem Studien-Arzneimittel in Zusammenhang stehen, ist dies zu protokollieren, indem der Randomisierungsdienst angerufen wird, der wiederum das CRASH Koordinationszentrum in London informiert. Im Allgemeinen müssen
Magen-Darm-Blutungen und Infektionen nicht auf diese Weise protokolliert
werden, da ein gewisser Anstieg ihres Auftretens bei Steroidgabe erwartet
werden kann. Gleichermaßen müssen die verschiedenen medizinischen
Vorkommnisse, die bei Patienten mit Kopfverletzung zu erwarten sind,
nicht per Telefon protokolliert werden. Alle diese Vorkommnisse werden
allerdings für alle Patienten routinemäßig auf dem Ergebnis-Formular
abgefragt. |
| 'Aufhebung der Verblindung' der zugewiesenen Behandlung im Notfall |
|
Im
Allgemeinen sollte nicht die Notwendigkeit bestehen, die Verblindung
der zugewiesenen Behandlung aufzuheben. Wenn sich Kontraindikationen
für Corticosteroide nach der Randomisierung entwickeln (z.B. schwere
Magen-Darm-Blutungen), ist die Versuchsbehandlung einfach abzubrechen.
Eine 'Aufhebung der Verblindung' wurde beim NASCIS-Versuch mit MP bei
Rückenmarkverletzung nie als nötig angesehen,[Ref
4] und sollte nur in jenen seltenen Fällen erfolgen, wenn
der Arzt glaubt, dass die klinische Vorgehensweise entscheidend von
dem Wissen abhängt, ob der Patient Corticosteroide oder Placebo
erhalten hat (z.B. bei Verdacht auf Anaphylaxe). In diesen wenigen Fällen,
in denen eine 'Aufhebung der Verblindung' für dringend notwendig
erachtet wird, ist der Randomisierungsdienst anzurufen, der Name des
Arztes anzugeben, der die Aufhebung der Verblindung autorisiert, sowie
die CRASH-Behandlungspackungsnummer (falls verfügbar). Dann wird
dem Anrufer gesagt, ob der Patient Corticosteroid oder Placebo erhalten
hat. |
Die
Haupt-Bewertungsmaßstäbe für die Ergebnisse sind:
Todesfälle im Krankenhaus, Komplikationen und kurzfristige Genesung sind auf dem Frühergebnis-Formular aufzuzeichnen, das mit Hilfe der Krankenhausaufzeichnungen vollständig ausgefüllt werden kann ¾ es sind keine zusätzlichen Untersuchungen erforderlich. Die langfristige
Genesung wird nach sechs Monaten entweder durch einen einfach per Post
verschickten Fragebogen ausgewertet, der direkt vom CRASH-Koordinationszentrum
zu den einzelnen Studienteilnehmern geschickt wird, oder per Telefon-Interview.
Dadurch entsteht keine zusätzliche Arbeit für die mitarbeitenden
Krankenhäuser. |
| Analyse |
|
Die Ergebnisse werden den Haupt-Bewertungsmaßstäben gemäß verglichen, wobei all jene, denen Methylprednisolone zugewiesen wurde mit all denen verglichen werden, denen Placebo zugewiesen wurde, auf der Basis der Behandlungsabsicht. Die Analysen werden stratifiziert nach der Zeitspanne, die zwischen der Verletzung und dem Beginn der Behandlung vergangen ist, und nach der Schwere der Kopfverletzung, wie sie mit der Glasgow-Coma-Scale bewertet wird. Bezüglich des Infektionsrisikos und des Magen-Darm-Blutungs-Risikos werden ebenfalls Vergleiche vorgenommen. |